 |
| △ 20160229_104633.jpg |
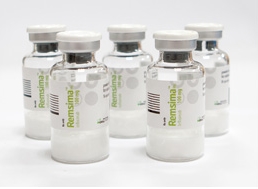
(서울=포커스뉴스) 셀트리온의 항체 바이오시밀러 램시마를 처방받은 유럽 환자가 올해 1분기 기준 약 8만2000여명을 돌파했다.
19일 셀트리온에 따르면 램시마는 지난해 말 기준 유럽 내 누적 처방환자 수 5만8000여명으로 유럽 오리지널 의약품 시장을 20% 잠식한 데 이어, 3개월 만에 약 2만3000여명의 처방 환자를 추가로 확보했다.
이는 유럽 내 램시마의 오리지널 의약품을 처방받는 자가면역질환자가 약 26만명으로 추산됨을 고려했을 때, 램시마가 오리지널 의약품 시장의 30%를 대체하고 있음을 나타내는 지표다.
특히 노르웨이에서는 지난해 램시마의 처방량 이 기존 오리지널의약품의 연간 처방량을 뛰어 넘는 등 오리지널 시장을 거의 100% 대체한 것으로 알려졌다.
램시마의 이 같은 선전은 유럽 내 주요국가들이 펼치고 있는 바이오시밀러 처방 장려정책에 따른 것으로 보인다.
영국은 NICE(The National Institute for Health and Care Excellence)를 통해 류마티스 관절염 및 강직성 척추염 환자의 바이오의약품 사용 시 가장 저렴한 인플릭시맙인 램시마를 우선 사용할 것을 권고한 데 이어, 바이오시밀러 처방률 제고를 위한 산업무역기구가 출범하는 등 활발한 바이오시밀러 처방 장려에 나서고 있다.
이탈리아의 경우, 의약품 가격 산정, 정책 수립 및 규제를 총괄하는 보건부 산하 기관 AIFA(Agenxia Italiana del Farmaco)가 세계 바이오시밀러 사용 및 지출 보고서를 발간하는 등 자국의 의약품시장 경쟁을 장려하기도 했다.
그간 바이오시밀러에 대해 교체처방을 허가하지 않았던 프랑스는 5월3일 의약품 판매 허가 기관인 ANSM(Agence Nationale de Sécurité du Médicament et des Produits de Santé)을 통해 오리지널 제품과 바이오시밀러 간 교체처방을 허가하도록 고시하는 등 각국의 바이오시밀러 처방장려 정책이 이어지고 있다.
셀트리온 관계자는 “램시마는 올해 유럽 오리지널 의약품 시장의 약 40% 이상을 점유할 것으로 예상된다”며 “램시마의 시장 점유율 증가에 대한 유럽 언론의 보도가 이어지는 등 램시마는 유럽에서 많은 관심과 호응 속에 순조롭게 처방과 판매가 이뤄지고 있다”고 말했다.
이 관계자는 또 “램시마의 유럽 판매 호조로 트룩시마와 허쥬마의 판매 파트너사 선정에 대한 관심도 고조되고 있다”며 “트룩시마의 허가일정을 고려해 3분기 중 후속제품의 유럽 및 미국 마케팅∙유통 파트너사 선정을 마무리짓고 론칭을 준비할 계획이다”라고 덧붙였다.<사진출처=셀트리온 홈페이지 캡처>
[저작권자ⓒ 부자동네타임즈. 무단전재-재배포 금지]